
背景介紹:
快速準(zhǔn)確地檢測(cè)臨床樣本中的多重生物標(biāo)志物對(duì)于提高疾病診斷、預(yù)測(cè)的準(zhǔn)確性和可靠性至關(guān)重要。得益于可編程性以及直接檢測(cè)核酸和非核酸靶標(biāo)的能力,CRISPR-Cas12a系統(tǒng)被認(rèn)為是一種通用且強(qiáng)大的多重生物標(biāo)志物分析技術(shù),通過crRNA與“啟動(dòng)子”核酸序列(ssDNA或dsDNA)的雜交激活CRISPR-Cas12a的反式切割活性后無差別的切割單鏈(ssDNA)報(bào)告子,根據(jù)報(bào)告子被切割后產(chǎn)生的信號(hào)變化便可實(shí)現(xiàn)對(duì)目標(biāo)物的檢測(cè)。盡管基于CRISPR-Cas12a的傳感體系已經(jīng)運(yùn)用到了多重生物標(biāo)志物檢測(cè),但仍面臨兩個(gè)不可忽視的瓶頸:(1)檢測(cè)多種不同的生物標(biāo)志物需要多種crRNA,增加了探針設(shè)計(jì)的復(fù)雜性和成本;(2)傳統(tǒng)ssDNA報(bào)告子之間的隨機(jī)碰撞導(dǎo)致切割反應(yīng)動(dòng)力學(xué)速率低,穩(wěn)定性差以及熒光染料的光漂白等問題都會(huì)導(dǎo)致檢測(cè)靈敏度不足,限制了其在復(fù)雜生物樣品中的應(yīng)用。因此,開發(fā)一種僅使用一種crRNA且具有高靈敏和高穩(wěn)定性的CRISPR-Cas12a傳感體系用于多重生物標(biāo)志物檢測(cè)具有重要意義。
針對(duì)上述科學(xué)問題,化學(xué)院羅細(xì)亮/徐升豪課題組基于前期等離子體激元共振增強(qiáng)熒光(PEF)的高靈敏精準(zhǔn)分子檢測(cè)的工作基礎(chǔ)上(Chem. Sci. 2024, 15, 566-572; Anal. Chem. 2024, 96, 16971–16977; Anal. Chem. 2024, 96, 4402-4409; Anal. Chem. 2023, 95, 3525-3531; Anal. Chem. 2022, 94, 5399-5405; Anal. Chem. 2022, 94, 16887-16893; Anal. Chem. 2022, 94, 14467-14474; Anal. Chem. 2021, 93, 2480-2489),開發(fā)了一種基于可編程DNA納米開關(guān)(NS)調(diào)控的等離子體CRISPR-Cas12a金納米星(Au-NST)報(bào)告平臺(tái),并且在空間限制效應(yīng)的輔助下實(shí)現(xiàn)了核酸和非核酸生物標(biāo)志物的檢測(cè)(圖1)。通過改變NS的識(shí)別區(qū)域序列,核酸(miRNA-375)和非核酸目標(biāo)物(PSA)均能打開NS使其暴露出相同的CHA觸發(fā)序列,經(jīng)過CHA反應(yīng)后釋放出相同的激活器(雙鏈DNA)并激活Cas12a,實(shí)驗(yàn)表明該設(shè)計(jì)僅需要改變NS的識(shí)別區(qū)域序列,便可利用一種crRNA實(shí)現(xiàn)兩種不同類型目標(biāo)物的檢測(cè)(圖1)。
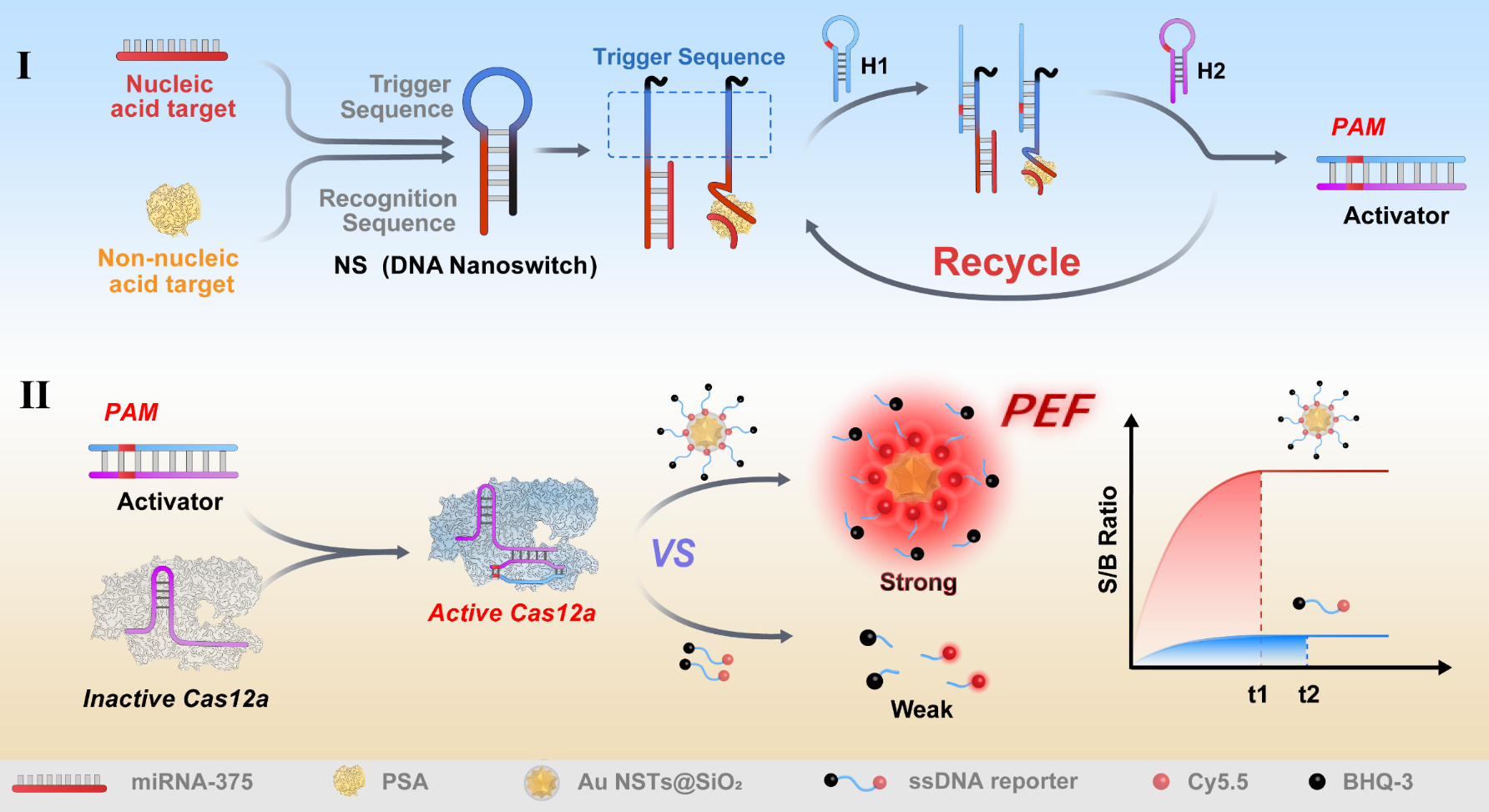
圖1可編程DNA納米開關(guān)調(diào)控的等離子體CRISPR-Cas12a平臺(tái)在空間限制效應(yīng)輔助下實(shí)現(xiàn)多重生物標(biāo)志物分析的示意圖。圖片來源:Nano Lett.
考慮到熒光染料的光漂白導(dǎo)致的靈敏度不足問題以及CRISPR-Cas 12a與傳統(tǒng)ssDNA報(bào)告子之間隨機(jī)碰撞導(dǎo)致的切割反應(yīng)動(dòng)力學(xué)速率低,穩(wěn)定性差等問題,我們制備了具有20個(gè)對(duì)稱“熱點(diǎn)”的金納米星(Au NST)并選擇其作為空間限制效應(yīng)和PEF基底,制備了Au NST報(bào)告子(圖2)。與傳統(tǒng)ssDNA報(bào)告子相比,Au NST報(bào)告子具有更快的反應(yīng)動(dòng)力學(xué),反應(yīng)時(shí)間從35min縮短至15min,熒光強(qiáng)度提高了近21.5倍。此外,由于球形核酸設(shè)計(jì),Au NST報(bào)告子對(duì)核酸酶(如DNase I)以及FBS的抗降解能力也得到了提升(圖3)。
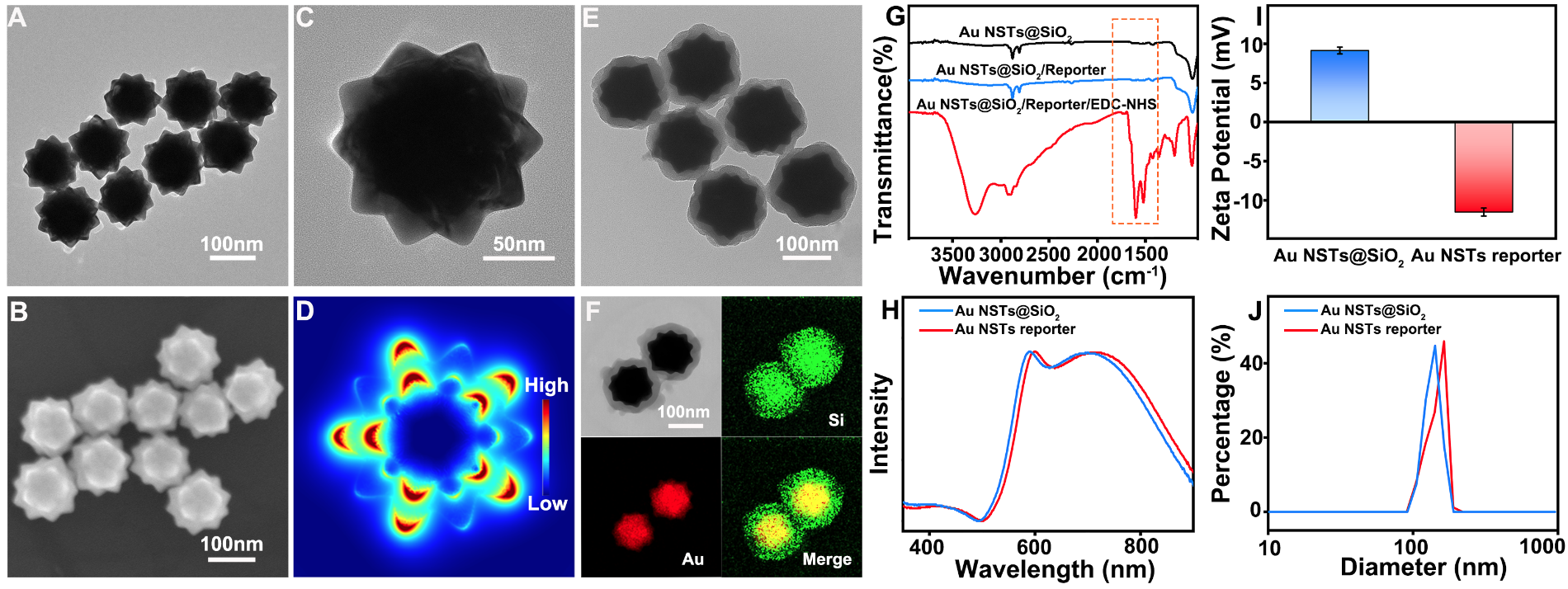
圖2 金納米星的透射電鏡、掃描電鏡等表征以及金納米星報(bào)告子的紅外光譜、Zata電位、吸收光譜及DLS表征。圖片來源:Nano Lett.
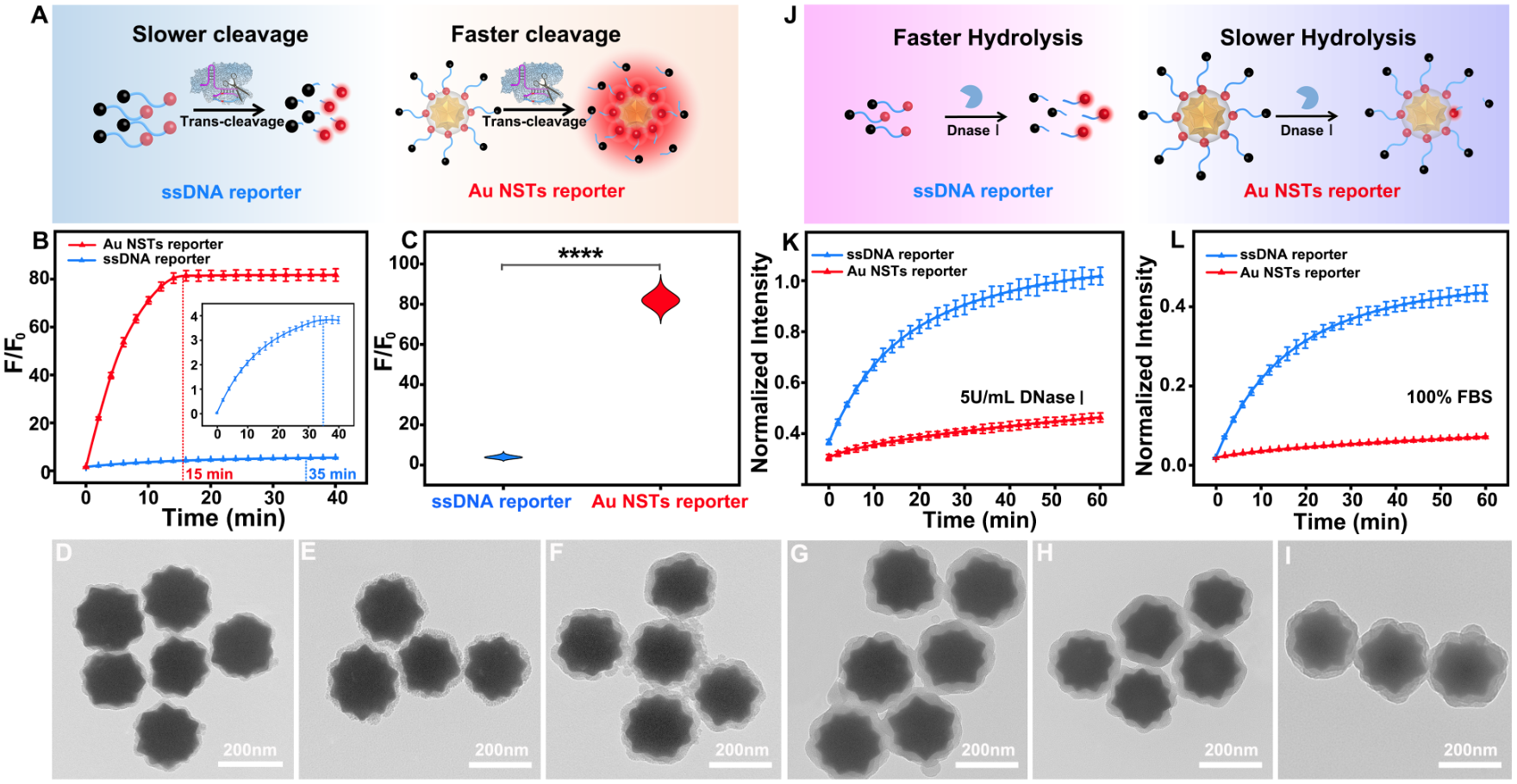
圖3 金納米星報(bào)告子與傳統(tǒng)ssDNA報(bào)告子的反應(yīng)動(dòng)力學(xué)及穩(wěn)定性對(duì)比。圖片來源:Nano Lett.
鑒于開發(fā)的NS調(diào)控CRISPR-Cas12a/Au-NSTs報(bào)告子具有出色的穩(wěn)定性和檢測(cè)性能,通過簡(jiǎn)單地改變NS的識(shí)別序列,進(jìn)一步評(píng)估了其對(duì)臨床尿液樣本中miRNA-375和PSA分析的實(shí)際檢測(cè)性能(圖5)。實(shí)驗(yàn)結(jié)果表明,該策略能夠?qū)崿F(xiàn)尿液中miRNA-375和PSA的高靈敏精準(zhǔn)定量檢測(cè),并能基于檢測(cè)到的這兩種尿液生物標(biāo)志物的差異表達(dá)水平成功鑒別健康人和前列腺癌病人,顯示了其在臨床應(yīng)用中的重要潛力。
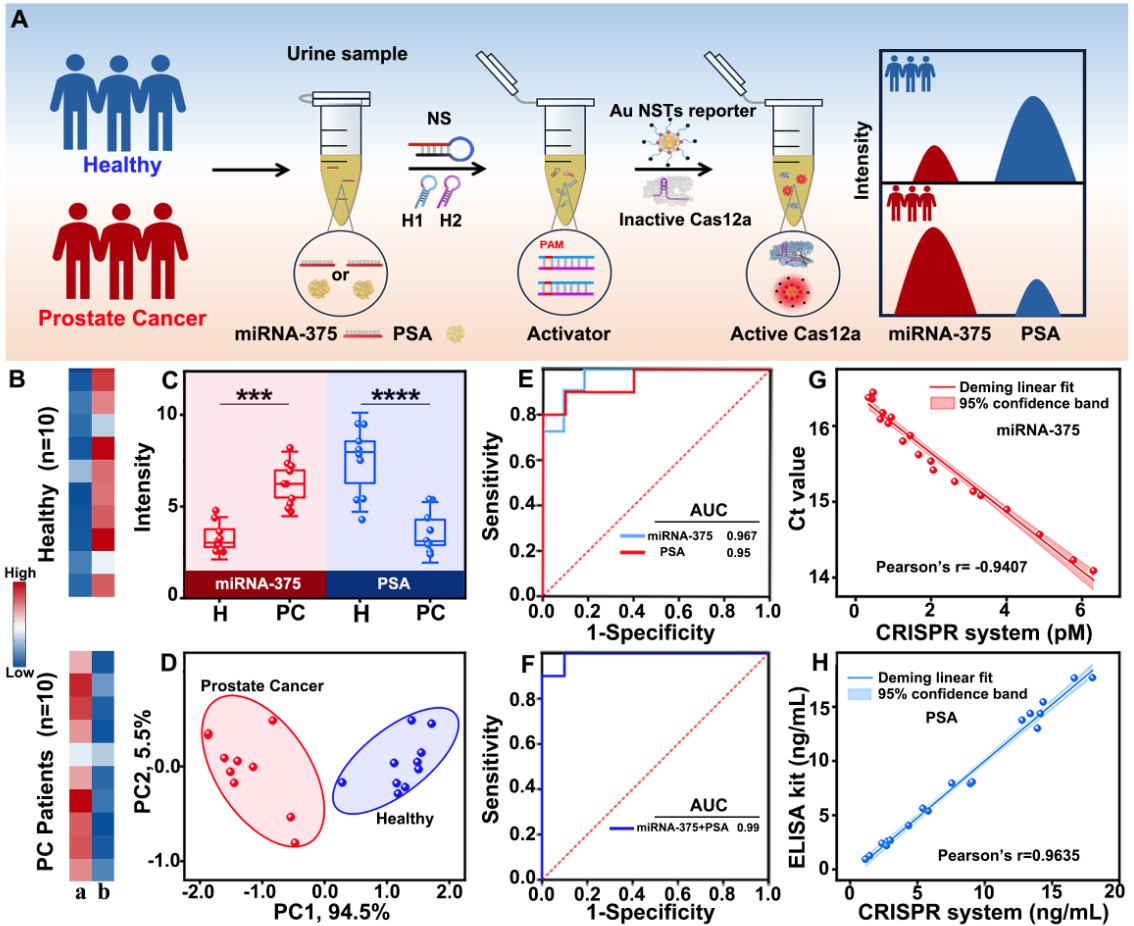
圖4 可編程DNA納米開關(guān)調(diào)控的等離子體CRISPR-Cas12a平臺(tái)對(duì)尿液中miRNA-375和PSA的檢測(cè)結(jié)果分析。圖片來源:Nano Lett.
該研究成果近期以題為《Programmable DNA nanoswitch-regulated plasmonic CRISPR/Cas12a-gold nanostars reporter platform for nucleic acid and non-nucleic acid biomarkers analysis assisted by spatial confinement effect》發(fā)表在Nano Letters上,文章的第一作者是2022級(jí)碩士研究生王從凱,通訊作者是青島科技大學(xué)徐升豪副教授和羅細(xì)亮教授。該研究得到國(guó)家自然科學(xué)基金(21505081、22374085))、山東省自然科學(xué)基金面上項(xiàng)目(ZR2023MB110)的資助支持。
論文信息:Congkai Wang, Xiaohan Xu, Wang Yao, Lei Wang, Xiaozhe Pang, Shenghao Xu,* and Xiliang Luo*, Programmable DNA nanoswitch-regulated plasmonic CRISPR/Cas12a-gold nanostars reporter platform for nucleic acid and non-nucleic acid biomarkers analysis assisted by spatial confinement effect, Nano Lett. 2025, DOI: https://doi.org/10.1021/acs.nanolett.4c05829






