腫瘤標志物成像技術是腫瘤診斷和治療的重要手段之一。基于小分子熒光探針的熒光成像技術因具有操作簡單、時空分辨率高、組織穿透能力強和無損檢測等優(yōu)良特性,已逐漸成為腫瘤標志物成像檢測中最具潛力的方法之一。目前,小分子熒光探針不同程度存在著發(fā)射波長短、易受生物背景熒光和自淬效應干擾,響應時間長,斯托克斯位移小,靈敏度較低等缺點。
針對以上問題,海洋科學與生物工程學院王曉春教授團隊長期致力于具有大斯托克斯位移,且對特定腫瘤標志物進行成像識別的近紅外熒光探針開發(fā),先后開發(fā)了能特異性監(jiān)控黑色素瘤標志物酪氨酸酶(Tyrosinase)和過氧化氫(H2O2)的高靈敏、高選擇性近紅外熒光探針(SensorsandActuators: B. Chemical,2022,354,131211;Sensors and Actuators: B. Chemical,2023,393,134301)。在此基礎上,該課題組以卵巢癌標志物β-半乳糖苷酶(β-gal)為切入點開展了系列研究工作,相關成果以“β-Galactosidase activity monitoring and bioimaging by a novel ICT mechanism-based NIR fluorescent probe with large Stokes shift”為題目發(fā)表在國際著名期刊《Sensors and Actuators B:Chemical》(JCR中科院一區(qū)Top)上(Sensors & Actuators: B. Chemical,2024,398,134696)。該論文第一作者為青島科技大學海洋科學與生物工程學院2021級碩士研究生高建,王曉春教授為獨立通訊作者,青島科技大學為第一通訊單位。
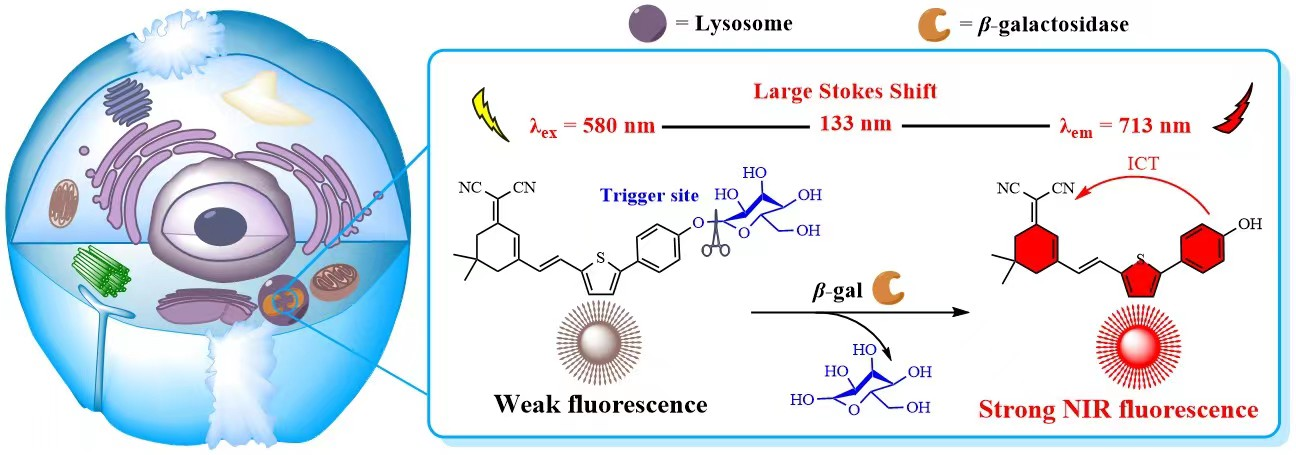
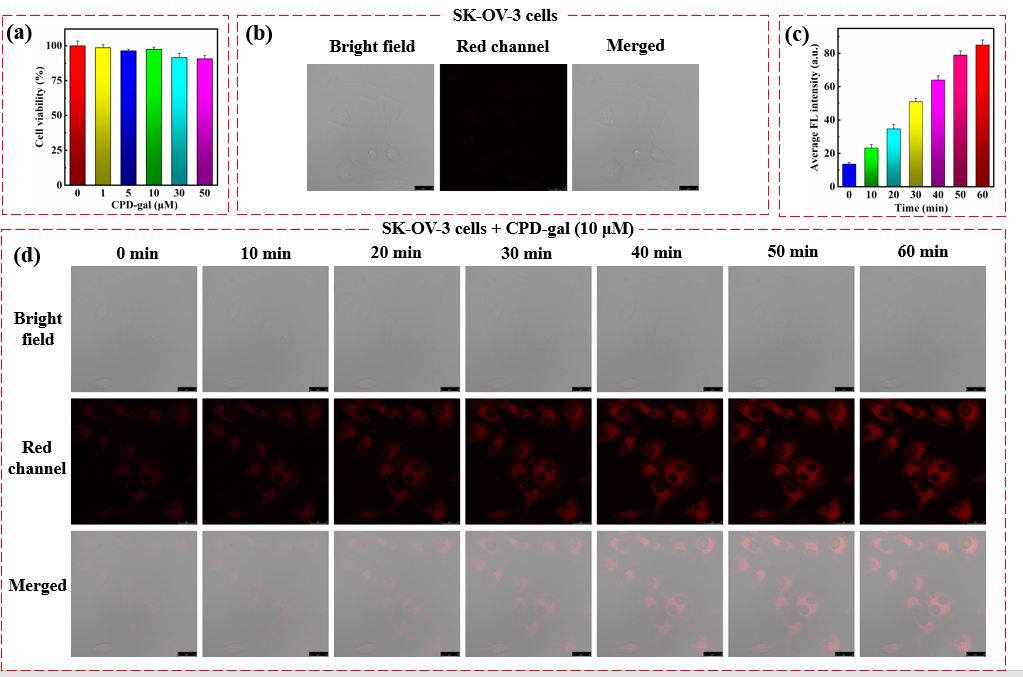
卵巢癌是威脅女性生命健康的重要疾病之一,早期的正確診斷是提高癌癥治愈率的關鍵。已有的研究表明:β-半乳糖苷酶(β-gal)作為原發(fā)性卵巢癌的重要生物標志物,是卵巢腫瘤可視化的重要分子靶點。我們以雙氰異佛爾酮衍生物CPD-OH為熒光母體,連接上半乳糖苷酶殘基構(gòu)建用于β-半乳糖苷酶(β-gal)識別的熒光探針分子CPD-gal。該探針母體CPD-OH具有較高的熒光量子產(chǎn)率(ФF= 0.31),基于ICT機理構(gòu)建的探針CPD-gal本身熒光淬滅,與β-半乳糖苷酶作用后,顯示出明顯的熒光增強效應。該探針具有近紅外發(fā)射(lem= 713 nm)、抗干擾能力強、靈敏度高(LOD = 6.0 ×10-4U/mL)、斯托克斯位移大(133nm)和細胞毒性低等優(yōu)點。利用該探針,我們成功實現(xiàn)了活體細胞(Hela cells和SK-OV-3 cells)和小鼠體內(nèi)的內(nèi)源性或外源性β-半乳糖苷酶的高分辨活體成像,為卵巢癌等疾病的早期診斷提供了有效手段。